Dimer lizozymu
Dimer lizozymu jest efektem procesu polimeryzacji pojedynczych cząsteczek naturalnego lizozymu białka jaja kurzego (ang. Hen Egg-White [HEW] Lysozyme).
Lizozym (muramidaza) należy do klasy enzymów hydrolizujących wiązania chemiczne i zgodnie z obowiązującą obecnie nomenklaturą systematyczną nosi nazwę N-acetylomuramido-glikano-hydrolazy. Odkryty został w 1922 roku przez szkockiego lekarza i mikrobiologa Aleksandra Fleminga - późniejszego laureata nagrody Nobla (1945). Enzym ten w naturze występuje powszechnie. Można go izolować z komórek i płynów ustrojowych wszystkich gatunków zwierząt, dlatego Fleming uważał, że odkrył naturalny, filogenetycznie bardzo wczesny, pierwotny mechanizm obronny, właściwy wszystkim żywym organizmom. U zwierząt występuje w kilku postaciach różnych dla poszczególnych podtypów taksonomicznych: typ c oraz typ g u kręgowców, a typ i (czasem także typ c) u bezkręgowców. U tych ostatnich, np. u pszczół, jest jednym z najważniejszych czynników naturalnej odporności, a charakterystyczny dla termitów i niezwykle istotny dla zaawansowanych społeczności tych owadów feromon rozpoznawania jaj TERP (ang. Termite Egg Recognition Pheromone) jest co do składu chemicznego i budowy identyczny z lizozymem.
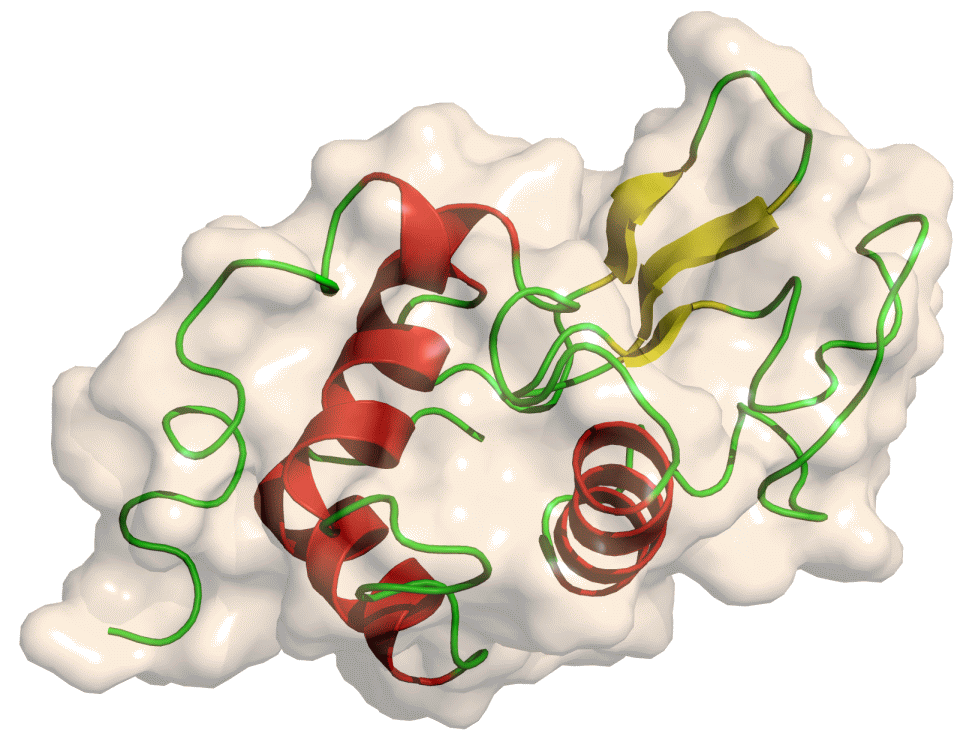
Struktura przestrzenna cząsteczki monomerycznego lizozymu ( X-ray structure pdb; Yikrazuul).
Jednocześnie z badaniami nad lizozymem Fleming prowadził intensywne prace z innym swoim epokowych okryciem – penicyliną. Kończąc pierwszy okres badań nad tą substancją i oddając ją do użytku klinicznego, wprowadził medycynę w zupełnie nową epokę – erę antybiotyków – ze wszystkimi ich zaletami i wadami. Świat stał wówczas u progu globalnej zawieruchy wojennej - II wojny św. i nowy lek miał wkrótce uratować życie tysięcy istnień ludzkich. Tym samym olbrzymi sukces penicyliny przyćmił pierwsze wielkie dokonanie Fleminga – odkrycie lizozymu, o którym głośniej stało się dopiero w 2 połowie XX wieku. Wówczas enzym ten stał się obiektem intensywnych badań biochemicznych, fizjologicznych i klinicznych. Jakkolwiek nie wszystkie jego właściwości zostały dotychczas poznane, to jednak wiadomo, że wykazuje on wyraźne działanie przeciwbakteryjne, przeciwwirusowe i przeciwzapalne.
To pierwsze polega na hydrolizie wiązań beta-1,4 glikozydowych pomiędzy kwasem N-acetylomuraminowym a N-acetyloglukozaminą, występujących w ścianie komórki bakteryjnej i prawdopodobnie może wymagać obecności lub współpracy innych enzymów bądź przeciwciał, co tłumaczy jego aktywność wyłącznie w żywym organizmie (in vivo).
Wiadomo również, że lizozym zawarty w lizosomach odpowiedzialny jest za wewnątrz komórkowe trawienie bakterii w fagocytach. Obecność lizozymu w komórkach żernych i jego wpływ na zjawiska fagocytozy potwierdziło wielu autorów, przy czym obserwuje się dosyć istotne różnice międzygatunkowe; np. ludzki lizozym stymuluje fagocytozę już w stężeniach fizjologicznych wynoszących 10-400 μg/ml, podczas gdy ten sam enzym izolowany z białka jaja kurzego wykazuje słabszą stymulację, którą można stwierdzić dopiero przy koncentracji 1000 μg/ml i wyższej.
Przeciwwirusowe właściwości lizozymu polegają prawdopodobnie na zwiększeniu odporności naturalnej i przypominają działanie interferonu (INF). Jest to raczej działanie pośrednie, polegające na pobudzeniu komórki do produkcji INF typu I (zwłaszcza INFα) raz typu II (INFγ), natomiast bezpośrednie oddziaływanie odbywa się na drodze połączeń dodatnio naładowanych cząsteczek dimeru z ujemnie spolaryzowanymi łańcuchami kwasów nukleinowych wirusa, tworząc nieaktywne kompleksy, zespolone wiązaniami elektrostatycznymi. Podobne związki lizozym tworzy z nukleoproteinami i lipoproteinami, które są niezbędne do rozwoju wirusów w komórkach.
W końcu lizozym wykazuje działanie przeciwzapalne; między innymi z uwagi na swoje silnie zasadowe właściwości neutralizuje kwaśne mediatory procesu zapalnego oraz obniża temperaturę ciała w przypadku, gdy proces ten wywołany jest przez endogenne pirogeny.
Wprowadzenie do lecznictwa preparatów zawierających naturalny monomeryczny lizozym nie dało jednak wyników terapeutycznych, jakich spodziewano się na podstawie teoretycznych rozważań. Oczekiwania te spełnił dopiero jego dimer, będący polipeptydem o masie cząsteczkowej około 27 tys. daltonów.
W warunkach naturalnych lizozym występuje prawdopodobnie wyłącznie jako monomer, ale stan ten warunkuje wartość pH, koncentracja i temperatura otoczenia. Zależnie od wahań tych parametrów, pojedyncze cząsteczki enzymu łączą się w dimery i wyższe polimery. Ulega przy tym zmianie nie tylko ciężar sumaryczny czy objętość nowej cząsteczki, ale także właściwości biochemiczne (więcej»). Z medycznego punktu widzenia jest to zjawisko korzystne, albowiem polimeryczna pochodna zachowuje kliniczną aktywność monomeru przy praktycznym wytrąceniu jego negatywnych właściwości, np. biotoksyczności. Molekuła dimeru lizozymu przybiera kształt sferyczny, będący cechą stałą, zależną od siły jonowej oraz wartości pH i przez to dającą się opisać w postaci prostego wzoru fizycznego. Uważa się, że dimeryzacja jest wstępem do odwracalnego procesu krystalizacji lizozymu, który można przeprowadzić w warunkach laboratoryjnych.
Zjawisko łączenia się monomerycznych cząsteczek w przyrodzie jest dosyć powszechne i wiele naturalnych substancji uaktywnia się dopiero pod postacią polimerów. Jako przykład mogą tu posłużyć immunoglobulina A oraz kachektyna, czyli czynnik martwicy nowotworów (ang. tumor necrosis factor; TNF), które występują zarówno w postaci zdimeryzowanej jak i trimeru, a immunoglobulina M jako pentamer. Aktywnym dimerem jest rybonukleaza nasienia buhaja, podobnie jak ludzka interleukina IL-5.
Badania firmy NIKA HP nad zastosowaniami dimeru lizozymu, opartego na polimeryzacji enzymu pozyskiwanego z białka jaja kurzego, były w medycynie ludzkiej i weterynaryjnej pionierskimi na skalę światową (więcej»). Potwierdziły one in vivo (na zarodkach kurzych), iż hamuje on całkowicie namnażanie się wirusa Sendai i to przy użyciu sto sunkowo niskiej dawki, bo wynoszącej 0,01 mg/ml. Równie silną inhibicję wykazuje w stosunku do wirusa grypy (wirus A/Sichuan nr 43/17), ospy krowiej i odry. Z tego względu należy przypuszczać, że dimer może być również skuteczny wobec innych wirusów, posiadających jednoniciowy, ujemnie spolaryzowany, segmentowany RNA; a więc także niedawno opisanego wirusa Schmallenberg i pozostałych ortobuniawirusów. Ponownie należy podkreślić, iż hamujący wpływ zdimeryzowanego lizozymu na chorobotwórcze drobnoustroje daje się zaobserwować wyłącznie w organizmach żywych.
Badania porównawcze dotyczące cytotoksyczności lizozymu względem fibroblastów kurzych dowiodły, iż dimer jest znacznie mniej toksyczny od swojego monomeru. Ten pierwszy nawet w stężeniu 1,0 mg/ml nie wykazywał żadnej cytotoksyczności do 7 dnia hodowli. Niezwykle niskie oddziaływanie toksyczne dimeru potwierdziły późniejsze badania na zwierzętach, gdzie pierwsze objawy nietolerancji występowały dopiero przy parenteralnym podaniu dawki powyżej 200 mg/kg m.c., (myszy szczepu NMRI) oraz powyżej 500 mg/kg m.c. u szczurów. Z kolei u psów obserwowano je dopiero przy zastosowaniu dawki 80 mg/kg m.c., a więc po przekroczeniu dawki leczniczej (0,02 mg dimeru lizozymu/kg m.c.) 4000 razy.
Jedną z niezmiernie ciekawych właściwości dimeru jest jego zdolność do modulacji syntezy wspomnianej już kachektyny (TNF), polipeptydu należącego do grupy cytokin i wytwarzanego głównie przez pobudzone makrofagi. Nie hamuje przy tym całkowicie jego syntezy, a jedynie zapobiega nadmiernemu wytwarzaniu, co z klinicznego punktu widzenia jest korzystne w wielu stanach chorobowych, np. ostrych zespołach biegunkowych czy w procesie nowotworowym.
Wprowadzenie dimeru lizozymu do lecznictwa weterynaryjnego stworzyło wiele nowych możliwości zapobiegania i leczenia szeregu jednostek i stanów chorobowych, zwłaszcza w połączeniu z innymi grupami leków, np. antybiotykami, w przypadku których dimer lizozymu znacząco obniża ich niekorzystne działanie immunosupresyjne.
Więcej na temat dimeru lizozymu na stronie Publikacje.



 Aktualności
Aktualności O firmie
O firmie Produkty
Produkty Immunostrefa
Immunostrefa Publikacje
Publikacje Szkolenia
Szkolenia Dimer lizozymu
Dimer lizozymu
 Opinie
Opinie
 Publikacje
Publikacje
 Rozprawy doktorskie
Rozprawy doktorskie
 Pliki do pobrania
Pliki do pobrania